版权所有- 江苏昆仲机械有限公司| Copyright - 2018 All Rights Reserved 苏ICP备17023086号
精馏中的三元相图解读
三元相图是共沸精馏或萃取精馏的基础,正确解读三元相图不仅能辅助我们选择合适的工艺路线,还能帮助我们在模拟流程中定量计算。
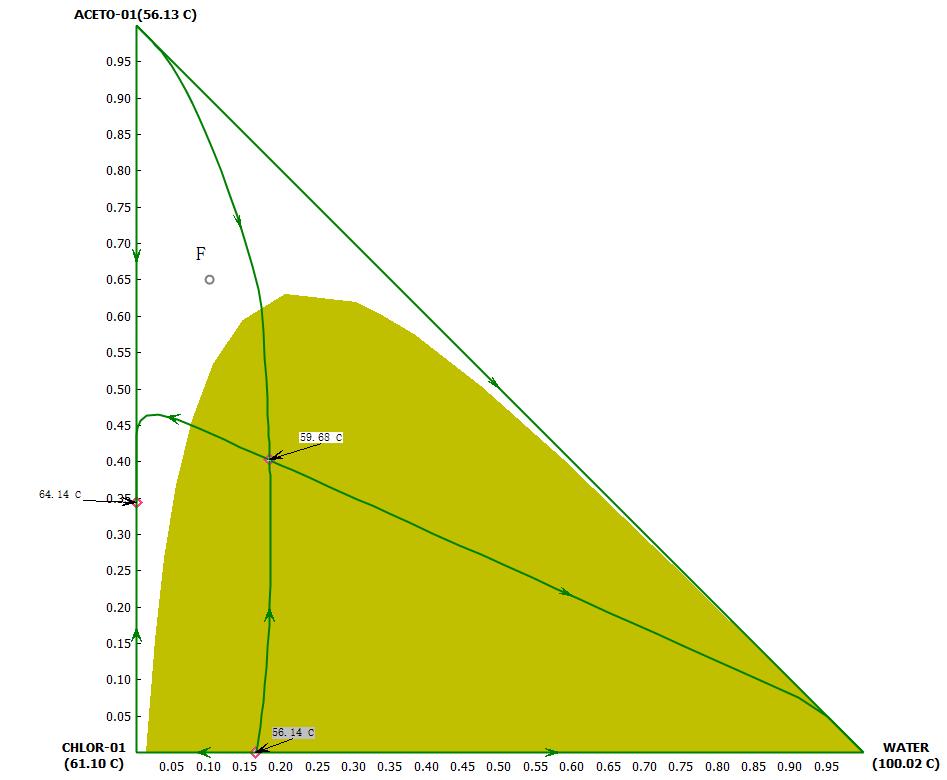
图1 典型的三元相图
三元相图表示可以用等腰直角三角形表示,也可以用等边三角形表示。以丙酮-氯仿-水为例,典型的三元相图直角三角形表示法如图1所示。组分1的摩尔分数(质量分数)在纵坐标上,组分2的摩尔分数(质量分数)在横坐标上。三个顶点分别表示三种纯物质,在纵横坐标两纯组分区间表示成分在0~1的组成。由于三个物质自由度为2,只要输入纵横坐标即可在图上确定此物系的唯一坐标点。如图中F点表示,10%摩尔分数的水,65%的丙酮和25%的氯仿。
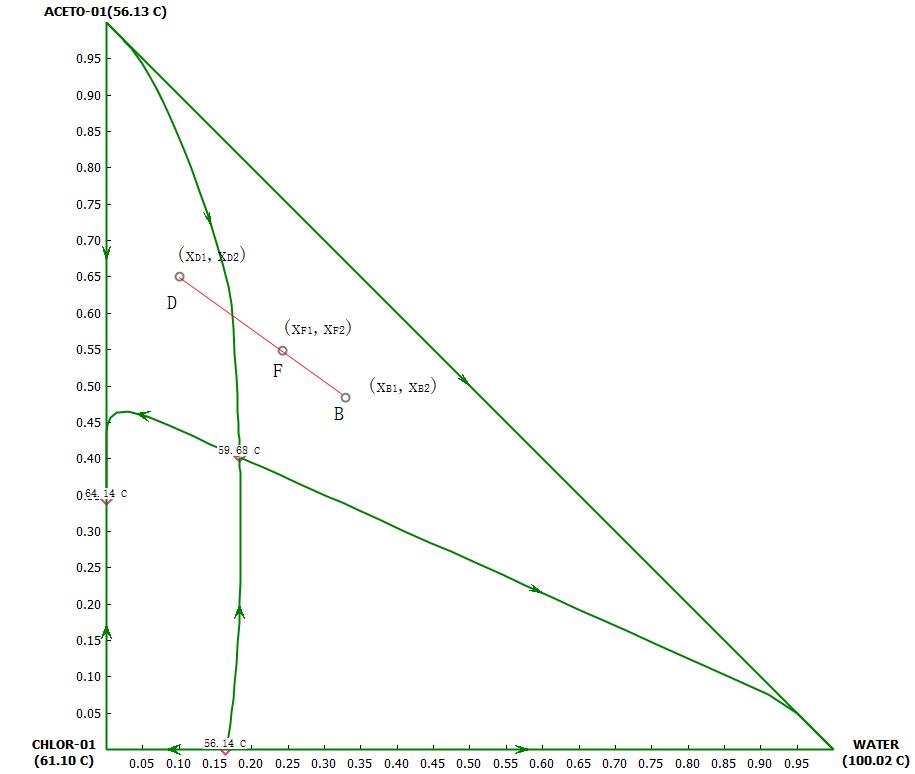
图2 三元相图中的混合规则
三元混合规则是三元相图中最有用的规则,已经有严格的数学证明,这里不再赘述。其大致原理如下图所示。即假如两股三元物流D、B混合,则混合后的组成在三元相图上,就处在两股物流对应坐标点的连线上。例如图2中,三元物流D对应的组成为xD1和xD2,三元物流B对应的组成为xB1和xB2,混合后的物流F组成xF1和xF2,处于点D和B坐标点的连线上。且物流D和物流B流量之比为BF:DF长度比,即为杠杆规则。
三元相图中另一个非常重要的概念就是剩余曲线。其定义可这么解读:在一个压力恒定的容器中,某三元混合物,初始组成为x10、x20,通过简单蒸馏的方法,将气相物流连续抽提出去,剩余液相中组成x1,x2的变化轨迹在相图上表示形成的曲线即为剩余曲线。
仍以丙酮-氯仿-水为例,说明如何利用ASPEN物性分析在三元相图上绘制剩余曲线的方法。
图3 “分析”工具栏
 图4 点击图中的“使用Distillation Synthesis三元图”
图4 点击图中的“使用Distillation Synthesis三元图”
在ASPEN组分输入完毕并选择物系方法后,在ASPEN主界面窗口的分析工具栏上点击选择“三元相图”或“残余曲线”,如图3所示。打开如图4所示的窗口,在此选择组分,气液、液液物性方法等。然后点击左侧“三元相图”打开如图5的窗口,要生成某个点剩余曲线,右击图形选择“增加”“曲线”选项。光标变为十字线,可停留在图上任意位置,并点击左键,就增加一条经过该点的剩余曲线,如图6所示。重复此步骤则可得到一组剩余曲线。
由图6可见,剩余曲线是有方向的,所有的剩余曲线都是始于最轻的组分,向最重的组分移动。同时也是温度升高的方向,起点对应于该区域内沸点最低的点,称为不稳定点(如图6中氯仿-水共沸点);终点对应于所在区域内沸点最高的点,称为稳定点(如图中水的沸点);既有箭头指向、又有箭头背离的中间温度的点叫做鞍点(如图中三元共沸点)。图6中所有残余曲线均始于最小共沸物,终于乙醇或水。其中一条特殊的残余曲线将三角形DE分为两个蒸馏区域,被称为精馏边界线。剩余曲线既不会相交,也不会穿越精馏边界线,每个精馏区域中的所有剩余曲线均始于相同的起点,终于相同的终点。
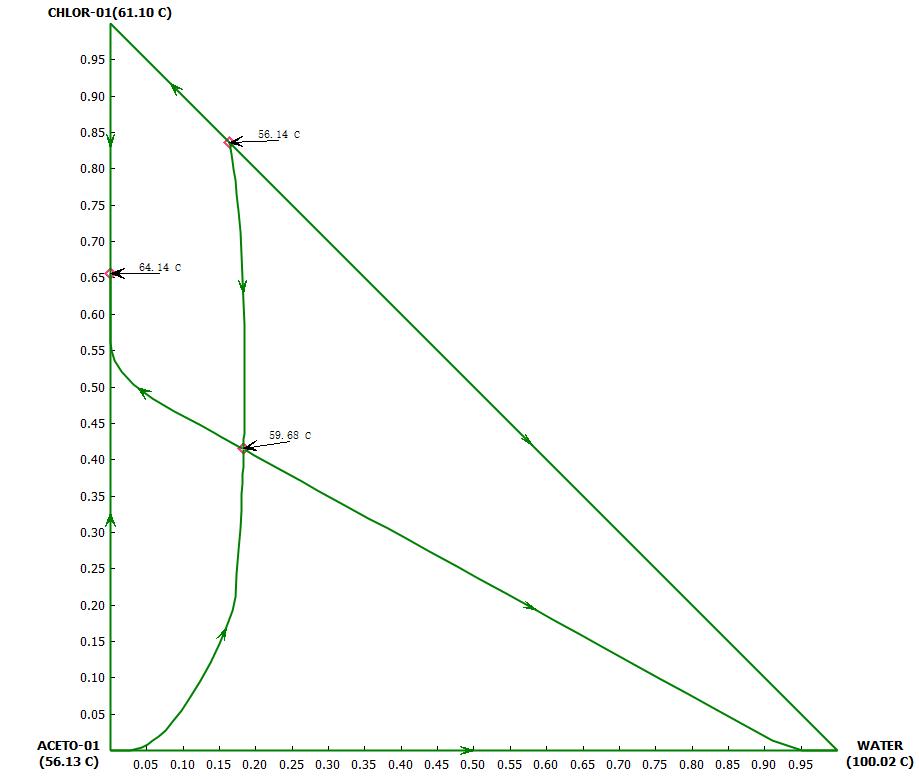
图5 “使用Distillation Synthesis三元图”打开的界面
 图6 剩余曲线
图6 剩余曲线
由于同一条剩余曲线上不同点对应这不同蒸馏时间,这与精馏塔内组成随塔板数变化类似,已有专著详细论证全回流状态下的无限高精馏塔塔内组分分布与剩余曲线表达式形式一致。这一关系提示我们可以利用剩余曲线评估一个给定系统的精馏分离方案的可行性。即一个可行性分离方案必须满足以下两个条件:
- 塔顶馏出物组成xD和塔底馏出物组成xB必须均位于同一条剩余曲线附近;
- 连接该两点的直线必须通过进料点xF。
精馏边界是另外一个比较重要的概念。在非理想性三元体系中,存在一个特殊的剩余曲线,它将三角形相图分为不同的区域,处于不同区域的组分得到不同的产品,这条特殊的剩余曲线就称为精馏边界线。可以这么理解,精馏分离三元组分时,受到共沸的限制,相图可划分为几个分离区域。当进料组成位于一个区域内,可得到确定的产品;当进料组成位于另一个区域时,可得到其他产品,这两个区域之间的分界线即为精馏边界。被精馏边界线分开的区域叫做精馏区域,同一个精馏区域内,所有的剩余曲线都有相同的起始点、终止点。不同的精馏区域内剩余曲线的起始点、终止点不同。根据精馏区域的这个特性,我们可以划分不同的精馏区域,而不同的精馏区域通过精馏手段只能得到被这个区域所包含的产品,而不能得到不被其包含的产品。
举例说明以上概念。
对一个三元体系而言,如果是理想体系,不形成共沸物。如甲酸-甲醇-水体系,其三元相图上无精馏边界,在整个摩尔分数范围内,剩余曲线具有相同的起始点(苯)指向相同的终止点(二甲苯),因此整个相图上就一个精馏区间,塔顶产物为苯,塔顶产物为二甲苯。如图7。
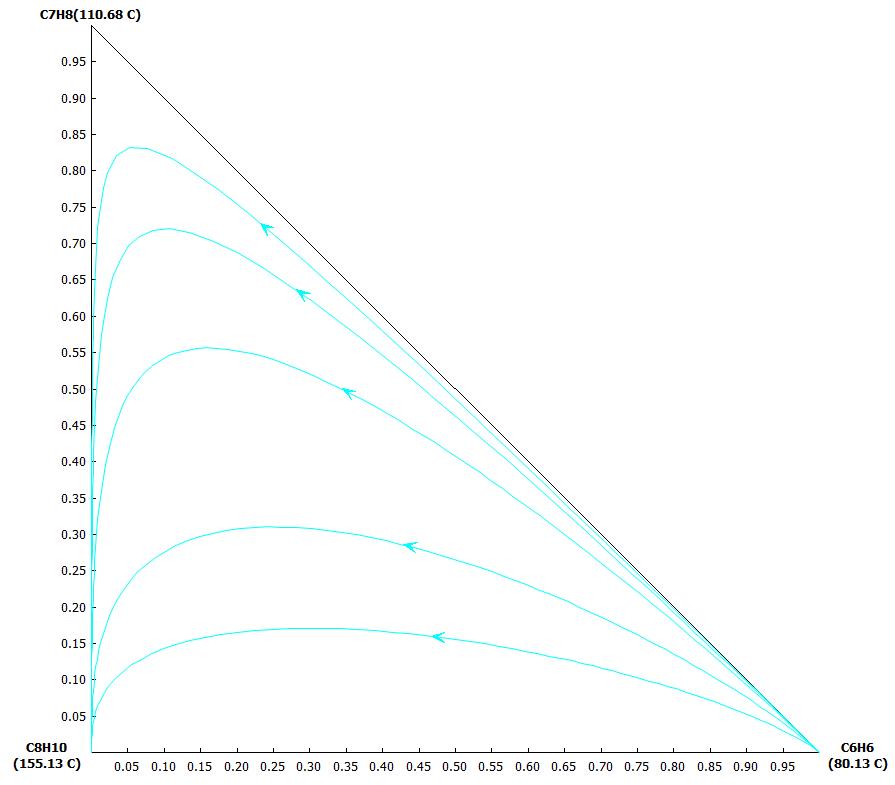
图7 苯-甲苯-二甲苯三元相图上不存在精馏边界线,剩余曲线总是从苯(最低沸点)指向二甲苯(最高沸点)
但是对一个非理想三元体系,如其中存在两个共沸的子系统,则该三元相图被分为两个区域。如正丙醇-异丙醇-苯体系(图8),该体系在常压下形成两个共沸物:异丙醇-苯最小共沸物(沸点71.65℃)和正丙醇-苯最小共沸物(沸点77.03℃)。该三元体系相图中精馏边界将相图分为左右2个区域。按前述定义,图中异丙醇-苯共沸点(71.65℃)是不稳定点,正丙醇沸点为稳定点,正丙醇-苯共沸点,异丙醇沸点都是鞍点。在右侧区域,苯的沸点是稳定点。因此,所有处于右侧蒸馏区的的残留曲线都终止于正丁醇顶点(沸点97.2℃);所有处于左侧蒸馏区的残留曲线均终止于纯苯顶点(沸点80.1℃)。如采用精馏分离此三元体系,当进料组成在左侧区域内时,我们可得到纯组分正丙醇,但无论如何,我们得不到纯苯,因为纯苯不在左侧这个精馏区域内。同理,进料在右侧区域内,通过精馏可得到纯苯,但得不到正丙醇和异丙醇,也是类似道理。
还有更复杂的体系,可将相图分为多个精馏区域,如乙酸乙酯-乙醇-水体系。该体系可形成3个二元共沸物和1个三元共沸物。将相图分成3个区域。三相共沸点(70.5℃)是不稳定点,乙醇-水共沸点,乙酸乙酯-水沸点,乙醇-乙酸乙酯沸点是鞍点,三个纯组分沸点是稳定点。如进料在左上方区域,通过精馏可得到乙醇纯组分,但得不到乙酸乙酯和水的纯组分。如进料在左下方区域,可得到乙酸乙酯纯组分,得不到乙醇和水纯组分。如进料在右方区域,可得到纯水,得不到乙醇和乙酸乙酯纯组分。
至此,我们已将三元相图中,比较难以理解的几个概念及其用途讲述完毕。还有个溶解度曲线虽然内容庞大,但不难理解。当相图中出现溶解度曲线时,又将给分离过程带来一波意想不到的结果。如有兴趣,可在以后的时间继续探讨。
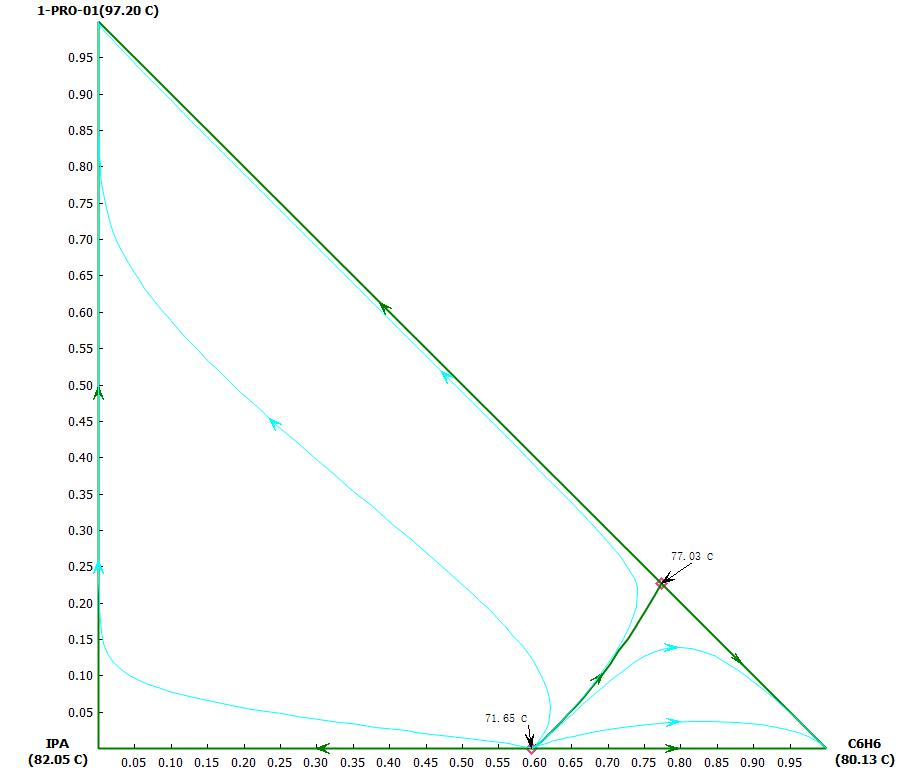
图8 苯-正丙醇-异丙醇三元相图
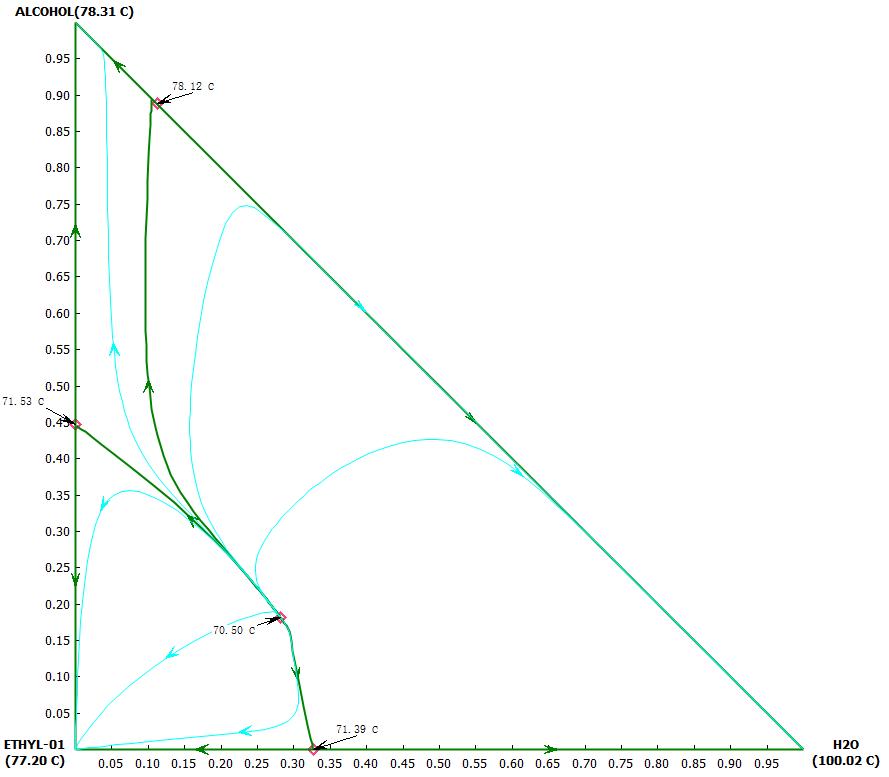
图9 乙酸乙酯-乙醇-水三元相图
最后欢迎同行指正,我们不回避错误,指出错误,意味着我们海川石化又有了努力新方向。




